問2 塩酸の電気分解で陰極と陽極で集まる気体の量が異なるのはなぜか。 塩酸を電気分解すると、水素と塩素が発生する。発生する量はじだが、塩素は水に溶け やすいので、集まる量が少なくなるから。(復習:化学反応式の係数で体積の比率が分かる) · 中和 ちゅうわ の化学反応式 マグネシウムに塩酸を加えると、塩化マグネシウムになり水素が発生する。 亜鉛と硫酸の反応 zn h 2 so 4 → znso 4 h 2 亜鉛に硫酸を加えると、硫酸亜鉛になり、水素が発生する。 そのほかの化学反応式一覧 エタノールの燃焼 c 2 h 5 oh化学式 通称 特長 塩化マグネシウム、 (塩化マグネシウム含有物) mgcl2・6h2o にがり(苦汁)塩マグ 凝固反応が瞬間的に起るため寄せ方が難しく、高度な技術と知識を必要とする 豆腐の味は最良 塩化カルシウム cacl2・2h2o 塩カル 凝固反応は塩マグとほぼ同じ 豆腐に使用した場合味が
中2理科 化学変化 テスト対策問題 Examee
塩化マグネシウム 化学式 なぜ
塩化マグネシウム 化学式 なぜ-理科2年 化学 分 解 原子分子 化合と化学反応式 酸化還元と熱 化学変化と質量 分解 要点-炭酸水素ナトリウムと酸化銀の分解 (1) 分解 :1つの物質が2つ以上の別の物質に分かれる化学変化。化学反応式 化学変化2 マグネシウムが燃えると,酸化マグネシウム ができる。 化学反応式 化学変化3 酸化銀を熱分解すると,銀と酸素ができる。 化学反応式 化学変化4 鉄と硫黄の混合物を加熱すると,硫化鉄がで きる。 化学反応式 化学変化5




5 Nhc1 Ca Oh Descubre Como Resolverlo En Qanda
塩化マグネシウムは Mgcl2と表されるのに水酸化マグネシウムはmg Oh 高校 教えて Goo 水酸化マグネシウムや水酸化銅 や水酸化鉄 はなぜこのよう Yahoo 知恵袋 酸化マグネシウムってなんで組成式なんですか 分子ではないんで Yahoo 知恵袋 中2☆ ここで書き並べたものは,すべてイオン反応式(イオン同士の結合の様子を式にしたもの)である。実際の化学反応式とは異なるものが多い。 例えば,(1)の塩化マグネシウムは,マグネシウムとうすい塩酸の反応 Mg + 2HCl → MgCl 2 + H 2 ↑ · マグネシウムオイル マグネシウムスプレー作り方 さらに 空気にふれたままになると ベタベタした液体になってしまいます。 塩化マグネシウムと精製水と1:1 でスプレーに使うのが良いかな? それ以上の 濃さで 乳液のように体にぬっても良いです。 き
塩化マグネシウムの化学式はMgCl 2 です。 1molの塩化マグネシウムには、Mg 2+ が1つと、Cl - 23 個)含まれています。 つまり、Mg 2+ 23 個」ですが1421 · 塩酸にマグネシウムリボンを入れて水素が出ていることを確認する実験です。 HCl→H + Clに電離します。 ここでMg2と、Clが結合します。 化学反応式の係数を併せる必要がありますね。 Mgが1、HClが2、これによってMgCl2が1になります。 またCl2つに合わせてHも2つになります。 水素ができました。 〈Mg+2HCl→MgCl2H2〉の完成です。塩化マグネシウム、硫酸マグネシウムは 強酸&弱塩基からなる塩だからです。 MgCl2→Mg2 + 2Cl となりますが、 Cl-は水中で安定ですが、Mg2が不安定で 一部が以下のような反応で酸性になります 酸性の水溶液の性質と特徴 は次の通り。 ①青色のリトマス紙を赤色に変える ②BTB溶液を黄色に変える ③鉄・マグネシウム・亜鉛(あえん) などの金属を加えると水素が発生
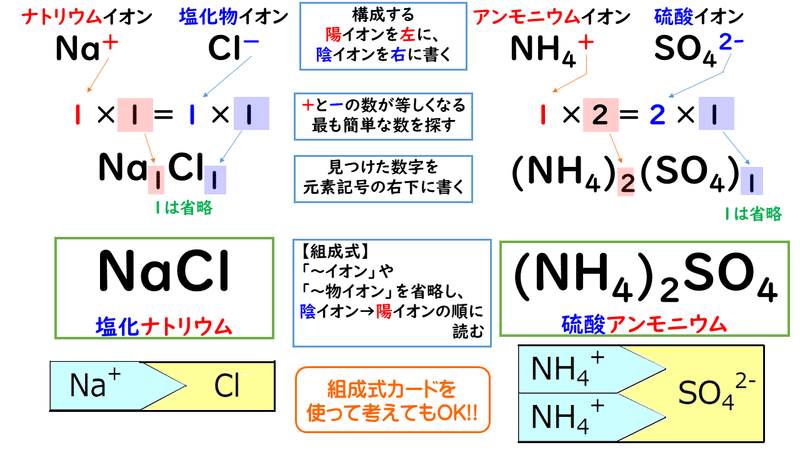
〇化学式→原子の記号を使って物質を表した式。 単体→1種類の原子だけでできている物質。 例(水素:H 2 酸素:O 2 銀:Ag 銅:Cu 鉄:Fe マグネシウム:Mg ) 化合物→2種類以上の原子からできている物質。 例(水:H 2 O 二酸化炭素:CO 2 塩化ナトリウム:NaCl 酸化銅:CuO化学式と組成式の違いがわかりません。 (2). 組成式の作り方がわかりません。 例 マグネシウム と 硫黄 ナトリウム と 二酸化炭素 亜鉛 と 塩素 (3). 組成式の作り方わかりません。<その2> 例 塩化物イオン と 銅イオン カルシウムイオン と 水酸化物イオン ナトリウムイオン と 酢酸イオン成分元素の原子の数を最も簡単な比で表した〔 組成式 〕という化学式で表す。 書き方 例) Ca 2 + と Cl - ・・・ Ca 2 + 〔 1 〕つと Cl - 〔 2 〕つの割合で結合 ① 陽イオンとその数,陰イオンとその数の順で並べる。 〔 Ca 2 + 1Cl - 2 〕




この化学反応式の意味を教えてください Clear



理科2年 化学
· 教養と学問、サイエンス > サイエンス > 化学 Wikipediaで化学について調べたところ塩化水酸化カルシウム、CaCl(OH) 塩化水酸化 塩化水酸化マグネシウム、MgCl(OH)は塩基性塩と書いてあったのですが、液性は不溶と書いてありました。 ほかのサイトではちゃんと液性がかいてあ りました。 結局これらの塩の液性は何をしめすのでしょうか?化学用 98% 500g ¥2,300 10~19本 ( 19:44 時点の在庫数) SDSファイル 日本語 ・ English 規格表ファイル 規格表 詳細情報 化学式 MgCl 2 構造 · 10/5/ 1156(編集あり) Ca^2とEBT (H3In)の錯体生成定数K=2・10^5はMg^2のK=10^7よりだいぶ小さい。 此が原因でCaEBT錯体は当量点より手前でEDTA (H4Y)と次のような反応を比較的緩やかに進めてしまう。 CaIn^ (赤) HY^3 → CaY^2 HIn^2 (青) 変色は緩慢だし誤差も生じ易い。 そこでEBTとのKは大きいが、EDTAとのKはCa^2の1/100程度と小さ




水の化学反応式は 2h2o 2h2 O2なのに なぜ酸化鉄の熱分解は 2ag2o 4 中学校 教えて Goo




塩酸はなぜか塩化水素酸と呼ばれない 化学がちょっとだけ好きな社労士
· 2個以上の原子が結びついてできる化合物は、重要なので1つずつ覚える。覚えないといけないおもな化学式は 水H2O 二酸化炭素CO2 塩化ナトリウムNaCl 酸化銅CuO 酸化マグネシウムMgO 塩酸(塩化水素)HCl 水酸化ナトリウムNaOH アンモニアNH3 など。1/121 覚えたい元素記号と化学式 何度も繰り返して覚えよう! 元素記号 は原子番号を示す。 44!これだけ覚えれば,大学入試も完璧です。 1水素 H 2ヘリウム He 3リチウム Li 4ベリリウム Be 5ホウ素 B 6炭素 C 7窒素(チッ素) N 8酸素 O 9フッ素 Fえんかマグネシウム塩化マグネシウム 化学式 MgCl 2 にがりの主 成分 ( せいぶん ) で, 純粋 ( じゅんすい ) でない 食塩 ( しょくえん ) が 潮解 ( ちょうかい ) 性 ( せい ) を示すのは,このため




5 Nhc1 Ca Oh Descubre Como Resolverlo En Qanda
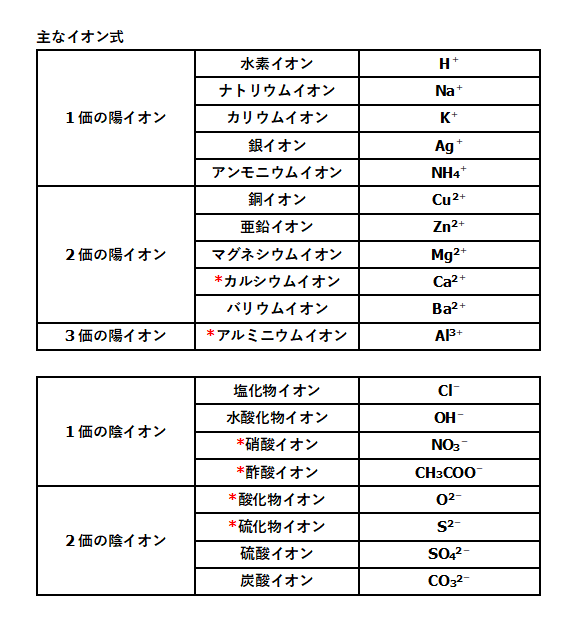



イオン式 電離式まとめ 中学理科 ポイントまとめと整理
· HClaqNaOHaq=NaClaqH₂O(液)56kJ 010mol/Lの塩酸500mL と 010mol/L の水酸化ナトリウム水溶液 500mL とを混合 させたとき, 発生する熱量は何kjか。 と言う問題で 答えが 56kj/mol × 010molL × 500/1000L=28kJ となっているのですが なぜこの式になるのでしょうか? 010molL × 500/1000L になる意味がよく分からないのでそこら辺を中心に教えていただきたいです。マグネシウムと塩酸が反応して、塩化マグネシウムと水素ができる実験を行います。 化学反応式は次のとおりです。 mg + 2hcl → mgcl 2 + h ;発皿に移して火をつけ,その結果を②と比べ,なぜ そうなるのか考える。 泡盛,赤ワインともに無色の液体が得られ,火を つけると淡い炎を出して燃える。 泡盛の蒸留では,「蒸留してできるのは水だから, 泡盛を蒸留すると熱い水が出てくる」と考える生徒 がいる。蒸留して




化学式塩化マグネシウム無水 Buy 塩化マグネシウム無水 化学式塩化マグネシウム 塩化マグネシウムの価格 Product On Alibaba Com




塩化マグネシウムは Mgcl2と表されるのに水酸化マグネシウムはmg Oh 高校 教えて Goo
化学反応式はhcl nh3 → nh4cl となり塩化アンモニウムが生成されます。 本来なら酸のh と 塩基の ohが反応をして水を生成するのですが、アンモニアには金 塩化ナトリウム 〔c〕化学式 ⑴ 分子からなる物質の化学式の書き表し方について, 教科書p28 を読みわかりやすくまとめなさい。 分子からなる物質の化学式の表し方 ② 水素・酸素など 水・二酸化炭素・アンモニアなど 中2理科家庭学習プリント⑬ 2年 組 番 名前: 教科書 p29化学成分 機械的性質 マグネシウム地金の製造法 電解法 用いられる原料の塩化マグネシウムの質などによって方法が異なります。 ダウ法 海水に石灰乳を加えて水酸化マグネシウムを沈殿させ、次に塩化水素を加えて塩化マグネシウムとしてから脱水処理した含水塩化マグネシウムを原料



中3化学 塩酸の電気分解 Sciencenote Jp
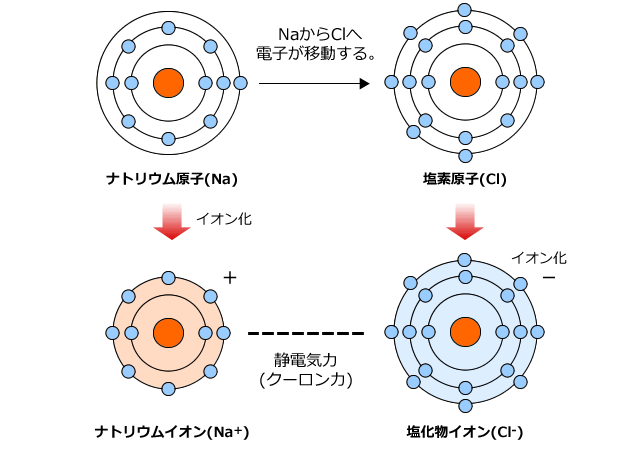



化学講座 第10回 イオン結合とイオン性物質 金属結合と金属結晶 私立 国公立大学医学部に入ろう ドットコム
· 化学 先日、塩化マグネシウムを生成しようと、マグネシウムの粉末と やや過剰量の濃塩酸を加えました。 マグネシウムがすべて溶けたので、あとは水溶液中の残った塩酸を、熱して気化させようとしました。Ph · その原理は、下の反応式のように金属マグネシウムが水と反応して水素を発生することを利用したものである。 2H 2 O + Mg → Mg(OH) 2 + H 2 金属マグネシウムの板を約5%のクエン酸水溶液に浸すだけで小さな水素の気泡が発生し続けるのを実験的に確認することができる。06 · 実験Bの3では、反応が終了するまで、そのままを維持する。 「解 説」 1水の中でも燃える: マグネシウムを空気中で燃焼させると、まばゆい光を放って激しく反応し、2Mg O 2 → 2MgO の反応が起こります。 燃焼中のマグネシウムを水につけてみると、たちまち熱が奪われるので、反応は停止してしまいますが、沸騰水だとかえって激しく反応し
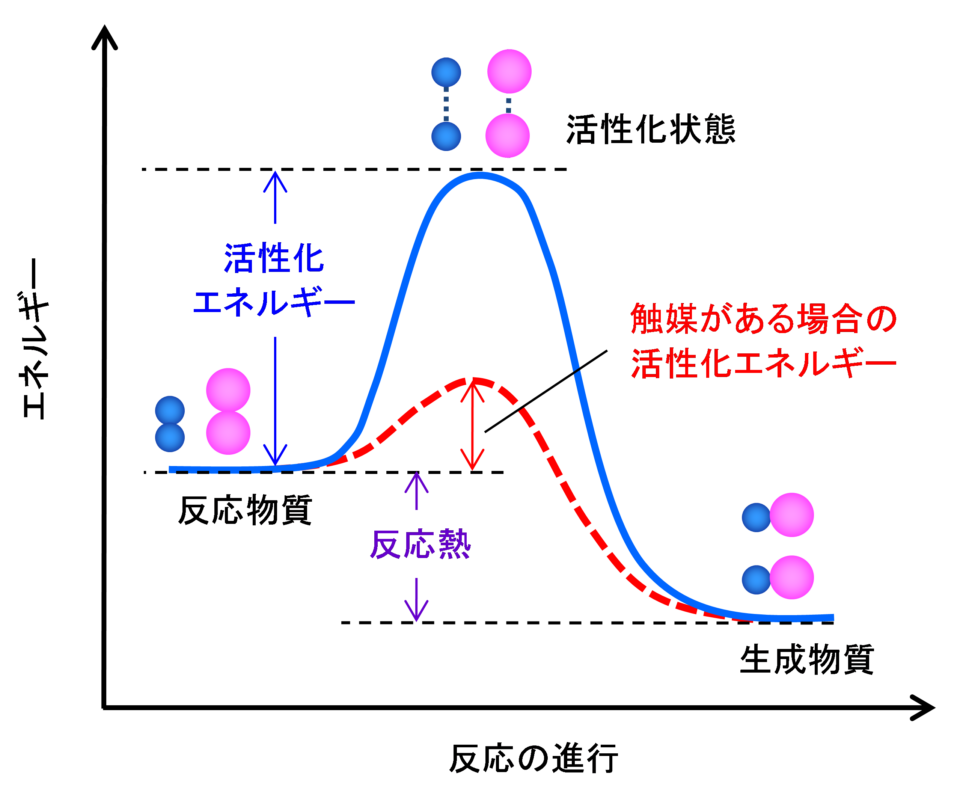



触媒とは何か 触媒工業協会




授業実践記録 化学 酸化還元反応の身の回りへの応用 亜鉛めっき をとおして 啓林館
えんかマグネシウム塩化マグネシウム magnesium chloride 化学式MgCl 2 。 海水から食塩を製造するときの副産物である苦汁(にがり)に含まれ,これから取り出されるほか,岩塩鉱床に存在するカーナリットKCl・MgCl 2 ・6H 2 Oを原料としても製造される。 ふつう6水和物MgCl 2 ・6H 2 Oとして存在する1901 · つまり、 化学反応式の完成 なんだね。 マグネシウムの燃焼の化学反応式 2Mg O 2 → 2MgO だね!1) 塩化マグネシウム Magnesium chloride,6-hydrate 化学式 MgCl2 ・6H2O = 3.30 成分含有量




至急です Clear




知ってると役立つ主要な化学式 英語 中国語 ピンイン付き 中国ビジネス支援のミツトミ株式会社
塩化マグネシウム〔無水〕 和別名6 エンカマグネシウム CAS RN ® メーカー名 キシダ化学 品位用途 含量 保存方法 容量 価格 在庫数;塩酸(塩化水素)はHClで、マグネシウムはMgです。 2つが反応すると塩酸の塩素とマグネシウムが化合して塩化マグネシウムとなります。すると塩酸の水素が残るので気体として出てきます。 ちなみに化学反応式は 2HCl Mg→MgCl 2H 2 です。高2化学です なぜ塩化マグネシウムの組成式にはカッコがなくて水酸化カル Yahoo 知恵袋 化学の組成式で 不定期に2とか3がついたり がついたり どうい Yahoo 知恵袋 高校の化学 組成式 組成式の作り方がわかりません 大至急です Yahoo 知恵袋 08 イオン結合 Youtube 組成式と分子式の違い 化学に




5 Nhc1 Ca Oh Descubre Como Resolverlo En Qanda




中2 理科 化学 化学反応式の作り方 22分 Youtube
2 塩化マグネシウム Ba2+ OH- hcl 塩化水素(塩酸) H+ NO 3 - hno 3 硝酸 H+ Cl- h 2 so 4 硫酸 K+ OH- koh 水酸化カリウム H+ SO 4 2- Na+ OH- naoh 水酸化ナトリウム Cu2+ Cl- 陽イオン 陰イオン 化学式 物質名 cucl 2 塩化銅 ① 陰イオン・陽イオンの順。0312 · 塩化マグネシウム(Magnesium chloride)は,化学式MgCl 2 で表される無機化合物です。 目次 Table of contents 1 塩化マグネシウムと不揮発性の酸が反応すると,揮発性の塩化水素が遊離します。 硫酸 との反応 MgCl 2 2 H 2 SO 4 Mg(HSO 4) 2 2 HCl ↑ 関連物質 Related substances 酸 塩化水素 Hydrogen chloride0以上 塩化マグネシウム 化学式 1325塩化マグネシウム 化学式 なぜ 高校化学基礎 過不足の計算1 映像授業のtry It トライイット 塩化マグネシウム 化学式 なぜ 塩化マグネシウム 化学式 なぜマグネシウム Wikipedia 楽天市場 化学式 塩化マグネシウムの通販



無機化学 沈殿生成反応



キリヤ Q A



1




混合物と純物質




塩化ナトリウムや酸化マグネシウムは単体 純物質 化合物 混合物




マグネシウムの燃焼 らくらく理科教室




2 マグネシウムmgを塩酸hclに加えると 塩化マグネシウムmgcl Clear




水溶液に硝酸銀水溶液を加えると白色沈殿を生じる 実験から塩素が確認される理由を アンサーズ



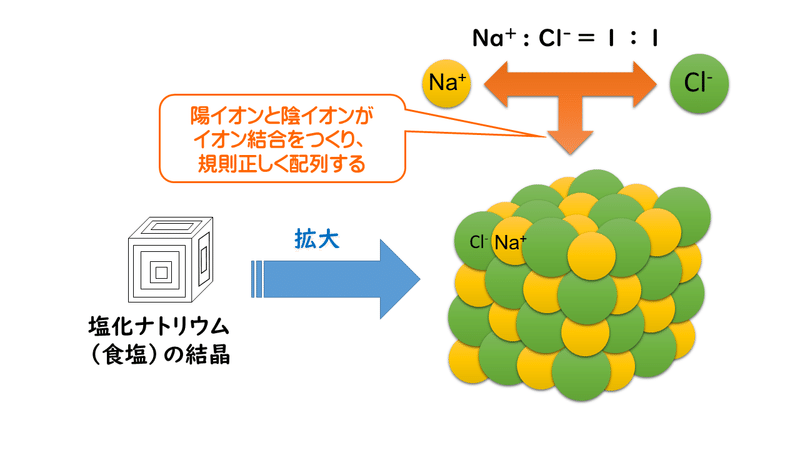
3 1 イオン結合とイオン結晶 おのれー Note




6 1 酸と塩基 おのれー Note



ヘリウム 化学式 ヘリウムってどんな物質 身近な例とともに化学系学生ライターがわかりやすく解説




4年保証 塩化マグネシウム500g 藤井薬品




カイロのすべて カイロのしくみ 桐灰カイロ 小林製薬




解説にある一番下の2 8 2は なぜ割る2をするんですか Clear



マグネシウムと希塩酸の化学反応式で 式の作り方自体はわかるのですが Yahoo 知恵袋



酸化銀の化学反応式について質問です 化学反応式にするとになるみた Yahoo 知恵袋




質量保存の法則とは フラスコを使った有名な実験とグラフ問題の解き方




中2理科 化学変化 テスト対策問題 Examee




中2理科 化学変化 だれでもわかる 化学反応式のつくり方 たけのこ塾 勉強が苦手な中学生のやる気をのばす



第1回 雪道に塩化カルシウム 株式会社 環境技術センター




知ってそうで知らない科学の話 海はなぜ塩辛いのか




塩化カルシウム 組成式




塩化カルシウム 組成式



2




塩化カルシウム 組成式 かっこ



中2理科です 酸化マグネシウムの化学式がmgoなのは何故ですか 酸 Yahoo 知恵袋



Q Tbn And9gctnf Kuuw2ywexw Pgennlhc2twnutae2kllzqsgrtll Azpbna Usqp Cau



3 1 イオン結合とイオン結晶 おのれー Note
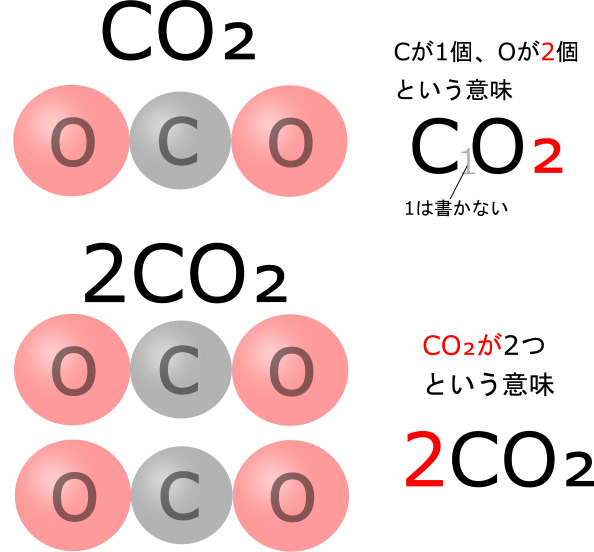



分子のできかたと分子をつくらない物質 理科の授業をふりかえる
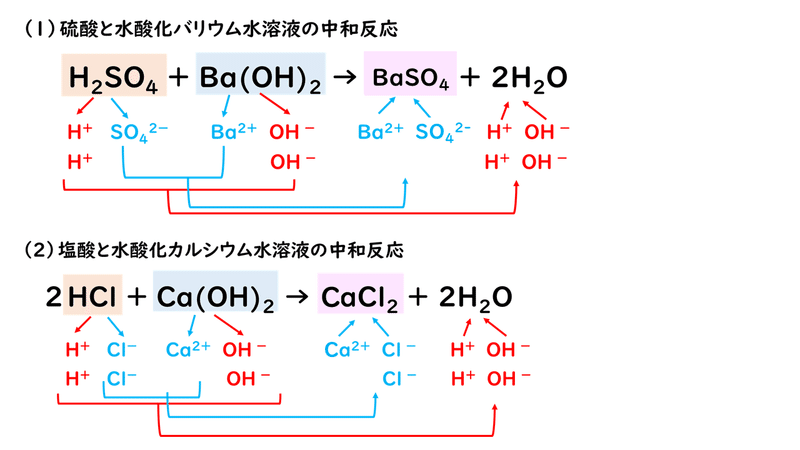



6 4 塩とその性質 おのれー Note




この反応でなぜこの答えになるのか分からないので教えてください Zai 化学 教えて Goo
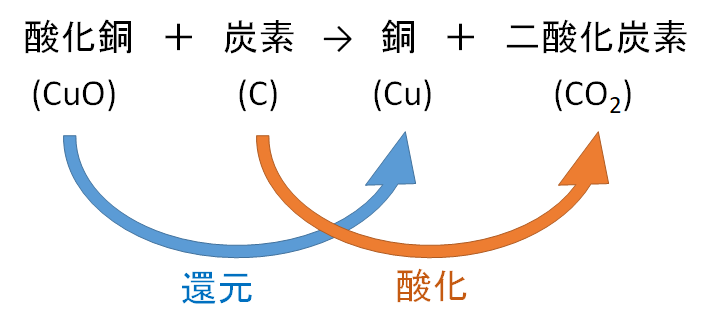



中2化学 還元 中学理科 ポイントまとめと整理




リン酸緩衝液のお話 Pb それともpbs
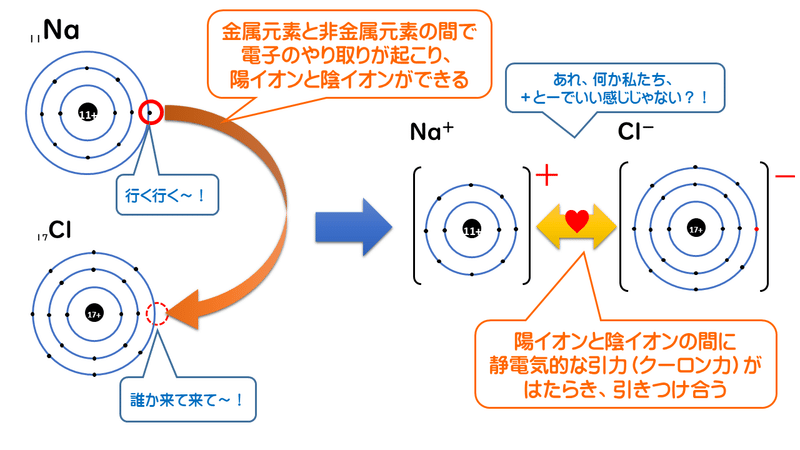



3 1 イオン結合とイオン結晶 おのれー Note




解説にある一番下の2 8 2は なぜ割る2をするんですか Clear
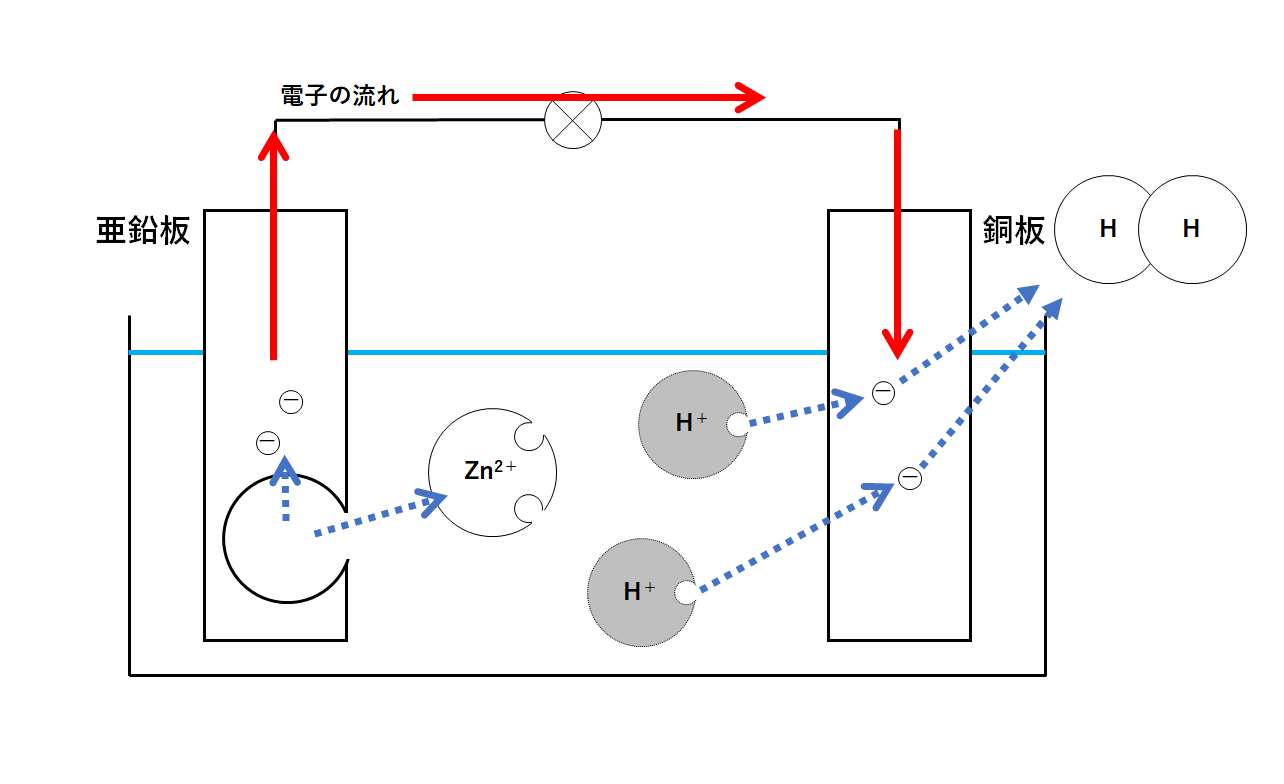



化学式 化学反応式 電離式のちがい 中学理科 ポイントまとめと整理



マグネシウムに塩酸を加えると 水素と塩化マグネシウムが生じる化学反応式を作っ Yahoo 知恵袋




間違えているところの解説お願いします 特に水酸化カルシウムに が 高校 教えて Goo



中2化学 炭酸水素ナトリウムの熱分解 Sciencenote Jp
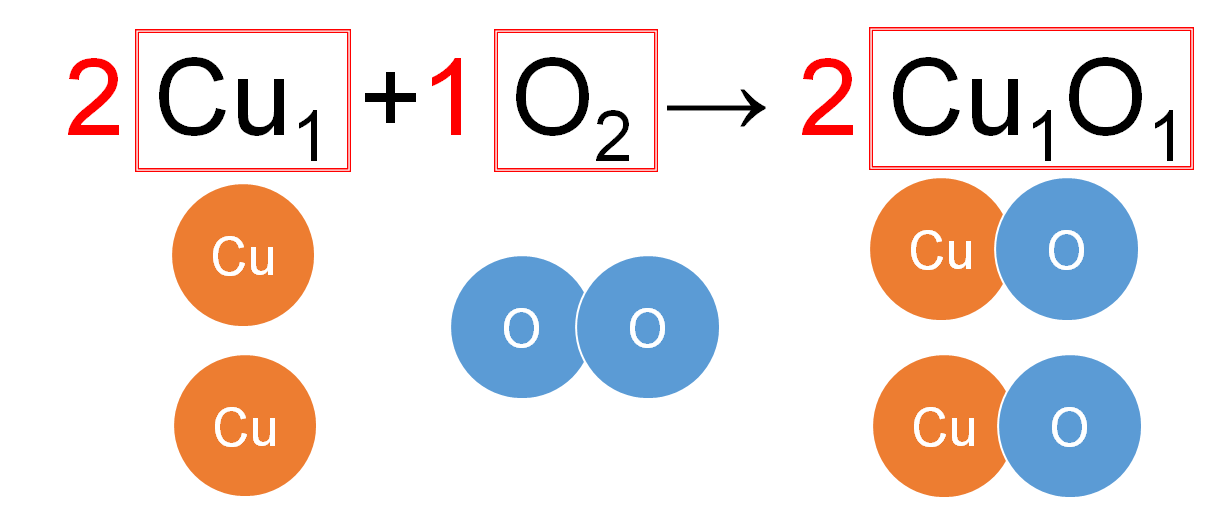



中2化学 質量保存の法則 中学理科 ポイントまとめと整理




イオン式 電離式まとめ 中学理科 ポイントまとめと整理
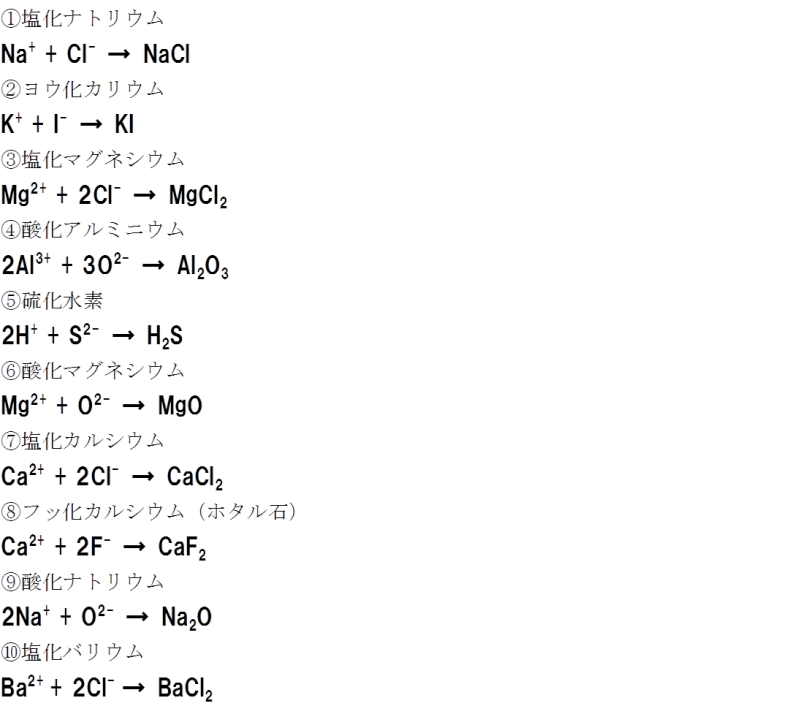



周期表を覚えると イオンがたくさん覚えられる 化学がちょっとだけ好きな社労士



マグネシウムの基礎知識 安全な取扱い 日本マグネシウム協会日本マグネシウム協会
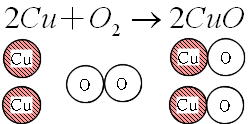



Science 化学変化と質量比 定比例の法則と原子量 分子量 働きアリ




有機化学 塩化ベンゼンジアゾニウムのnについてなのですが Nって 化学 教えて Goo




分子のできかたと分子をつくらない物質 理科の授業をふりかえる




塩基性塩化マグネシウムの意味 用法を知る Astamuse




5 Nhc1 Ca Oh Descubre Como Resolverlo En Qanda



3




右辺の化学式をどのような化学反応をさせることで左の様な化学式が得ら 化学 教えて Goo
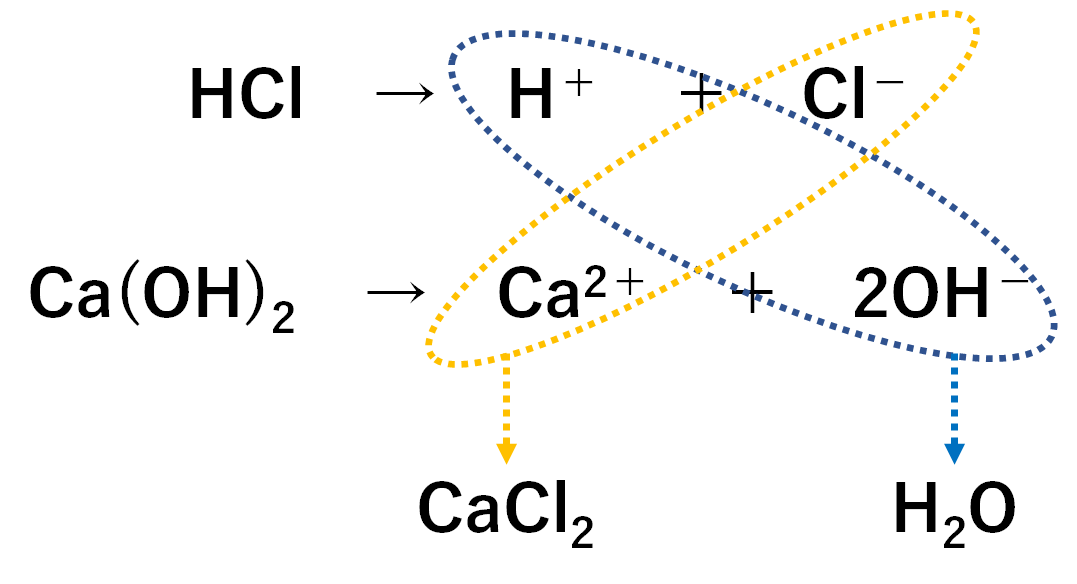



中3化学 中和反応 中学理科 ポイントまとめと整理




一問一答式 化学2年 化学変化と質量




塩化カルシウム 組成式
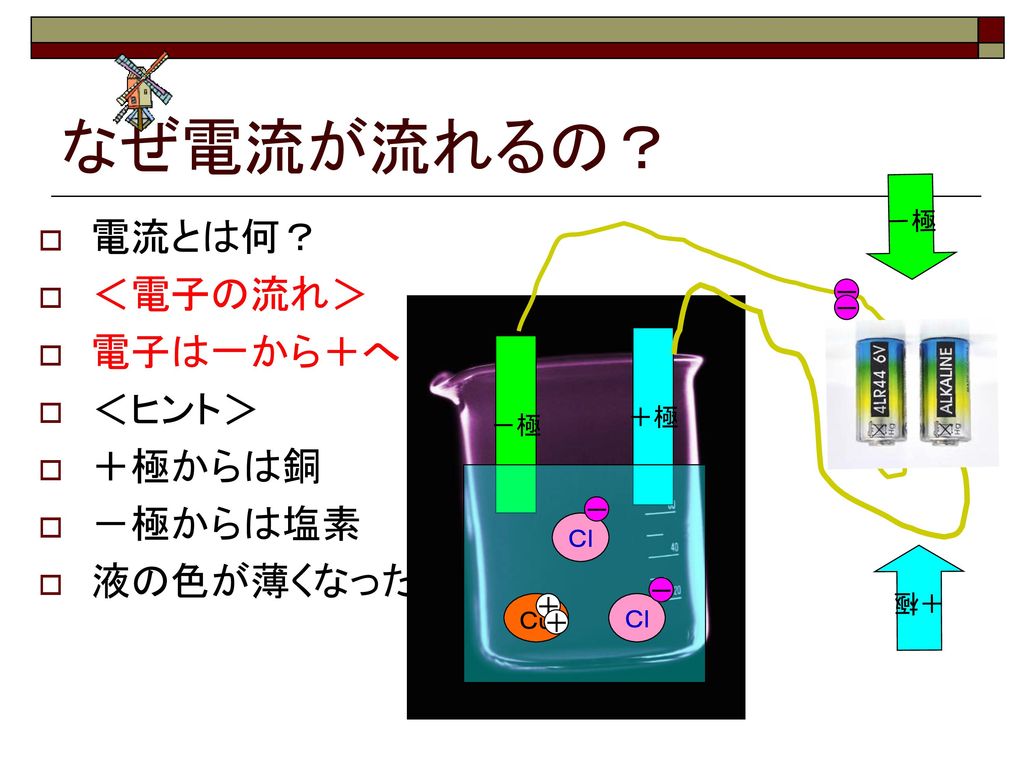



化学変化とイオン イオン って何だろう アルカリイオン飲料 マイナスイオンで健康に 化学変化 とはどういう関係 Ppt Download




塩化マグネシウム Wikipedia




なぜ塩化銅の化学反応式は画像の赤字のようになるのでしょうか Clear
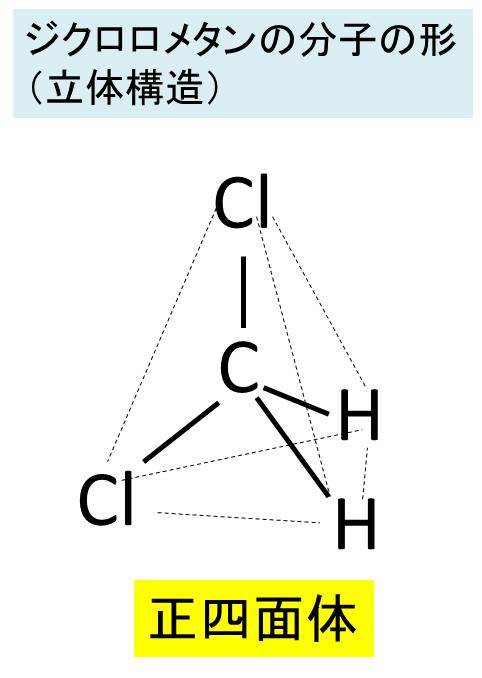



ジクロロメタン 塩化メチレン の分子構造 立体構造 は 極性を持つ理由は 極性溶媒



2




2 マグネシウムmgを塩酸hclに加えると 塩化マグネシウムmgcl Clear




海水はなぜ錆びやすいのか 関東塗料工業組合




塩化カルシウム 組成式 かっこ




この化学反応式の意味を教えてください Clear




写真のポリカーボネートの合成で 塩化水素が2n Mol になるのはなぜで 化学 教えて Goo



2




うすい塩酸にマグネシウムリボンを入れると 水素が発生するのは なぜですか Clear



高2化学です なぜ塩化マグネシウムの組成式にはカッコがなくて水酸化カル Yahoo 知恵袋



1




化学の質問です ジアゾニウム塩の化学式はなぜ符号が付いているので 高校 教えて Goo



Http Www Fdtext Com Dan Fdn 2k1 Genshi Pdf
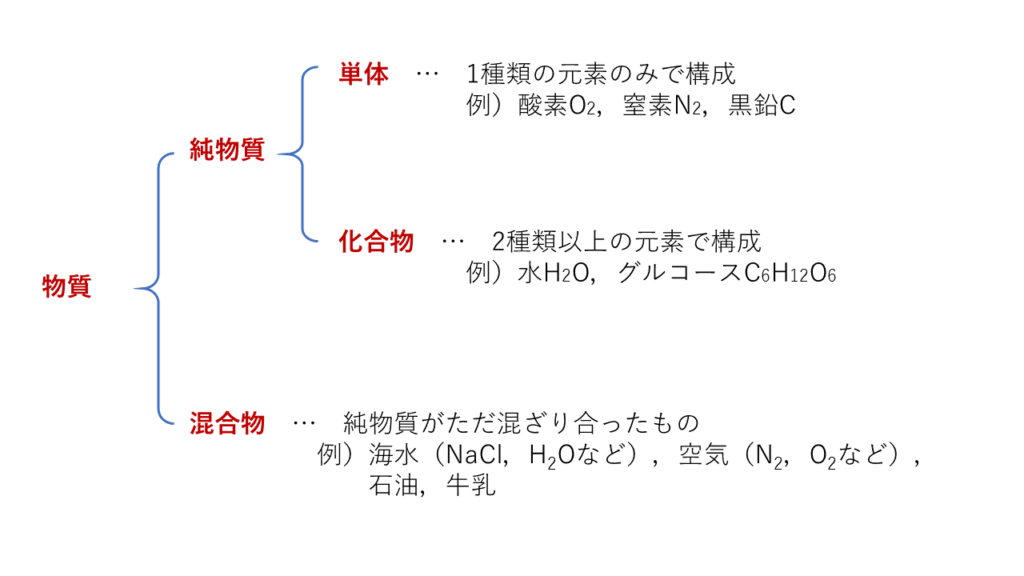



3分でわかる 単体 化合物 純物質 混合物の違いの見分け方と具体例を練習問題つきで解説 サイエンスストック 高校化学をアニメーションで理解する
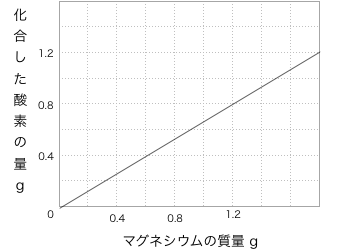



質量保存の法則とは フラスコを使った有名な実験とグラフ問題の解き方




アンモニアの分子式は Nh ですが アンモニウムイオンのイオン式は Nh アンサーズ



このマグネシウムの燃焼の化学反応式についての質問です マグネシウムはm Yahoo 知恵袋
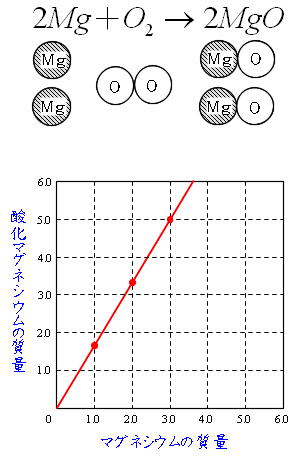



Science 化学変化と質量比 定比例の法則と原子量 分子量 働きアリ




化学反応式 中学生の学習法 Shun Ei Note




728 350g Descubre Como Resolverlo En Qanda




至急お願いします 調べても出てこず 解説動画を見ても全然分かりません Clear




豆腐 豆乳ってなんで にがり で固まるの 豆腐レシピの豆腐ラボ



キリヤ Q A



中3化学 塩化銅水溶液の電気分解 Sciencenote Jp



塩化マグネシウムとは何 Weblio辞書




2 1 G 10 18 Lihat Cara Penyelesaian Di Qanda




海水はなぜ錆びやすいのか 関東塗料工業組合




中2理科 分子をつくらない物質 映像授業のtry It トライイット




永遠の定番実験 マグネシウムの還元 酸化反応



塩化カルシウム 組成式 かっこ
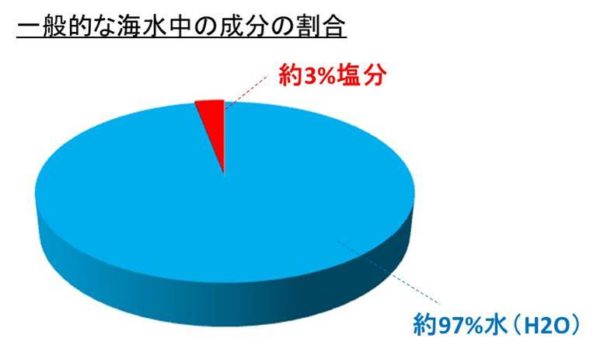



海水や死海の塩分濃度はどれくらい 作り方を解説 モッカイ



塩化水酸化マグネシウム Mgcl Oh の電離式はどのようになり Yahoo 知恵袋



0 件のコメント:
コメントを投稿